北大刘志博团队在《Nature》首次揭示核素探针诱导细胞焦亡的抗肿
2020年3月11日,北大化院应用化学系刘志博实验室和北京生命科学研究所邵峰实验室合作在Nature杂志在线发表题为A bioorthogonal system reveals antitumour immune function of pyroptosis的文章。在前期工作中,刘志博实验室发现一类含硼氨基酸探针(18F-硼氨酸)在肿瘤上有显著且特异的摄取,并将其用于临床中脑瘤的早期诊断和精确划界。在该项研究中,研究人员发现硼氨酸上的三氟化硼基团可直接用于硅烷(silyl ether)的脱除反应。在此基础上,研究人员在细胞以及活体水平上构建了苯丙硼氨酸(Phe-BF3)介导的生物正交剪切系统,赋予硼氨酸探针激活功能,并通过“双靶向激活”策略实现了肿瘤选择性的蛋白功能调控。该系统具有普适性,但对于需要在肿瘤细胞内选择性释放的蛋白更具优势,而Gasdermin蛋白就是一个范例。邵峰实验室近年研究发现Gasdermin家族蛋白是细胞焦亡的执行分子。Gasdermin蛋白在细胞内被激活后,其N端结构域在细胞膜上寡聚成孔,最终导致细胞裂解性死亡,诱导强烈的炎症反应。研究人员将该生物正交系统应用到Gasdermin蛋白后,实现了肿瘤原位且可控性地激活细胞焦亡。进一步研究发现,在肿瘤中引发细胞焦亡可诱导机体高效的抗肿瘤免疫活性进而清除肿瘤。
在活体内实现肿瘤选择性的蛋白功能调控,对生命科学研究和临床药物开发都有着非常重要的意义,但目前仍是化学生物学领域一个长期存在的挑战。该研究工作一方面展现了基于三氟化硼脱硅反应的“双靶向激活”策略效率高、生物正交性好的优势,揭示了将探针改造为激活剂(Probing-to-Perturbing)这一设想在活体蛋白激活上的巨大潜力。利用这个新颖的生物正交技术,该研究揭示少部分的肿瘤细胞发生焦亡,就足以有效调节肿瘤免疫微环境,进而激活很强的T细胞介导的抗肿瘤免疫反应,该发现为肿瘤免疫治疗药物研发提供了新的思路,Gasdermin家族蛋白也成为潜在的肿瘤免疫治疗的生物标志物,这类蛋白的激动剂则很有可能成为抗肿瘤药物研发的新方向。
刘志博实验室的博士生王钦阳和邵峰实验室的博士后王玉鹏是本文的共同第一作者,该论文的其他作者还包括中科院生物物理所的丁璟珒博士,刘志博实验室的研究生王春洪和交流生周雪涵,邵峰实验室的研究生高文清和黄焕伟,北京大学刘志博博士和北京生命科学研究所邵峰博士是本文的共同通讯作者。该研究由中核集团-国家自然科学基金联合基金,中组部青年千人计划,北京分子科学国家研究中心,北大-清华生命科学联合中心,中科院战略先导科技专项,科技部重点研发计划,及中国医科院创新医学单元项目,在北京大学和北京生命科学研究所完成。
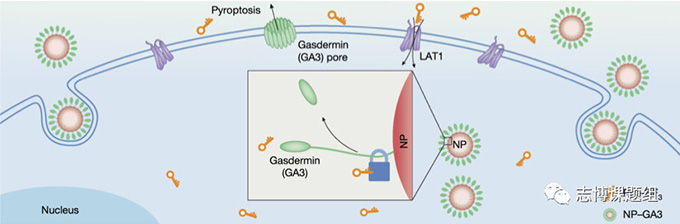
图一 硼氨酸介导的生物正交剪切系统在细胞内可控释放Gasdermin蛋白示意图。
相关文章: