单剂211At标记抗HER2 单域抗体片段有效治疗人乳腺癌模型
编者案:近日,杜克大学医学中心在Journal of Nuclear Medicine发表了一种基于治疗核素At-211标记抗HER2单域抗体片段的靶向α粒子治疗策略。引起编者的兴趣,在与作者联系后,选译其中部分,分享给业内人士!
本研究采用了两种可与HER2领域IV高亲和力结合的sdAbs(5F7和VHH_1028),考察了HER2靶向sdAbs与iso-211At-SAGMB结合物对表达HER2的人乳腺癌的疗效。

Effective Treatment ofHuman Breast Carcinoma Xenografts with Single-Dose 211At-LabeledAnti-HER2 Single Domain Antibody Fragment
标题:单剂211At标记抗HER2单域抗体片段有效治疗人乳腺癌模型
Title:Effective Treatment of Human BreastCarcinoma Xenografts with Single-Dose 211At-Labeled Anti-HER2 Single DomainAntibody Fragment.
Authors:Feng Y, Meshaw R, ZhaoXG, Jannetti SA 3rd, Vaidyanathan G, Zalutsky MR.
Journal:JNM,2022,DOI: 10.2967/jnumed.122.264071.
(选译,版权归属JNM 杂志,本译文仅供参考)
研究的通讯作者为杜克大学癌症研究所Michael R. Zalutsky教授,第一作者为杜克大学医学中心助理教授冯钰天博士。该研究得到了CA42324和Cereius公司的基金支持。
研究背景:
人表皮生长因子受体2型(HER2)在乳腺癌、卵巢癌和胃癌中过度表达,并经常与转移性进展相关。尽管HER2靶向治疗可以提高生存率,但对这些治疗的抗性经常发生。此外,这些药物对脑转移无效,而脑转移是HER2阳性乳腺癌越来越普遍和致命的后果。出于以上原因,我们迫切需要具有不同作用机制并适合脑内病灶给药的靶向治疗方法。
靶向α粒子治疗(TAT)是一种新型的癌症治疗策略,它能够通过与目前已批准的HER2靶向药物不同的机制发挥细胞毒性作用。此外,其50-100微米的辐射范围与高细胞毒性相结合,使α粒子有望在最大限度减少对周围正常组织的毒性的同时用于辐射转移灶。然而,完整抗体的大尺寸导致了肿瘤内传递的缓慢和不均匀、以及在正常组织中的长时间停留。
为了解决这些局限性,单域抗体片段(sdAbs;又称纳米抗体或VHH)正在被作为TAT的替代骨架进行评估,其中HER2可能是研究最广泛的目标分子。HER2来自骆驼科动物,分子量仅为12-15kDa,且具有纳摩尔或亚纳摩尔的亲和力,并表现出低免疫原性。与完整的抗体相比,sdAbs的肿瘤穿透更快,而且能成功地递送到HER2阳性的脑瘤中。已有用225Ac和213Bi粒子标记HER2领域I靶点2Rs15d可行性的报道,但也观察到肾脏的高摄取。
用放射性卤素211At标记这种抗HER2的sdAb,具有更有利的肿瘤相对肾脏的摄取比。此外,211At的半衰期(7.2小时)与sdAbs的药代动力学非常匹配。另一方面,砹-211每次衰变只发射一个α粒子,没有混杂的粒子反冲效应,而且其合理的成本也增加了可用性。
研究方法:
使用N-琥珀酰亚胺-3-211At-砹-5-苯甲酸胍基甲酯(iso-211At-SAGMB)对HER2特异性sdAbs和与HER2无关的VHH_2001进行标记。比较了iso-211At-SAGMB-5F7和iso-211At-SAGMB-VHH_2001对表达HER2的BT474乳腺癌细胞的毒性。在皮下注射BT474异种移植物的小鼠身上进行了三次实验,以评估单剂量的1)iso-211At- SAGMB-5F7(0.7-3.0 MBq),2)iso-211At-SAGMB-VHH_1028(1.0-3.0 MBq)和3)iso-211At-SAGMB-VHH_1028和iso-211At-SAGMB-VHH_2001(约1.0 MBq)的治疗效果。
iso-211At-SAGMB-sdAb的放射合成和质量控制:
通过改变反应体积、反应时间、乙酸水平和正相HPLC柱的进样量,对~370MBq 211At反应的程序进行了优化。从最初的211At到iso-211At-SAGMB-sdAb结合物的总合成时间为3.5h,总的放射化学产率为16.1±7.0%。 iso-211At-SAGMB-sdAbs的摩尔活性为1.74-4.41 MBq/nmole。iso-211At-SAGMB-sdAbs的SDS-PAGE荧光成像显示了一个对应于预期分子量约13kDa的单一放射性带(补充图1),RCP为97.6±0.8%(n=9)。
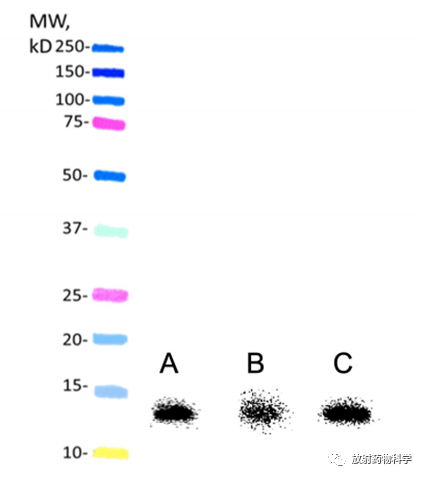
补充图1. 211At 标记sdAbs的SDS-PAGE荧光成像。A. iso-211At-SAGMB-5F7; B.iso-211At-SAGMB-VHH_1028; C. iso- 211At-SAGMB-VHH_2001
细胞存活率测定:
在集落形成试验中比较了iso-211At-SAGMB-5F7和HER2非反应性iso-211At-SAGMB-VHH_2001对BT474细胞的细胞毒性。确定iso-211At-SAGMB-5F7的D0(将存活率降至37%的活性浓度)为1.313 kBq/mL。同时测量了iso-211At-SAGMB-VHH_2001对照组的细胞毒性,没有观察到存活率的降低(图1),证明iso-211At-SAGMB-5F7的细胞毒性是HER2特异性的。
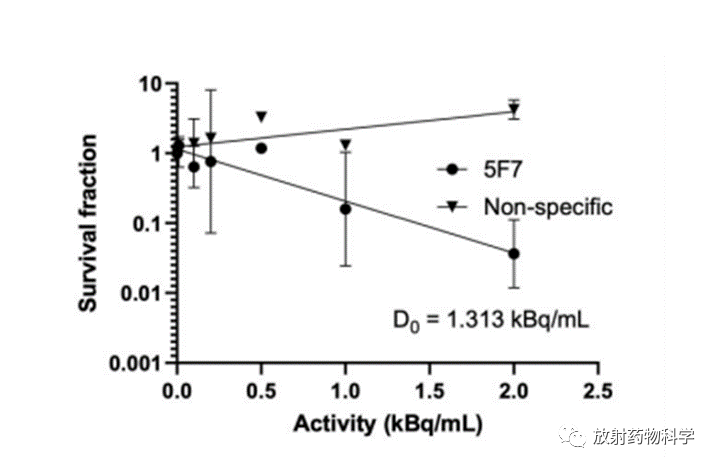
图1. BT474乳腺癌细胞与iso-211At- SAGMB-5F7和与HER2非反应性的iso-211At-SAGMB-VHH_2001培养后的存活率。
生物分布和剂量测定:
皮下BT474异种移植的雌性裸鼠通过静脉注射iso-211At-SAGMB-VHH_1028(200 kBq/1 µg,100 µL PBS)。注射后1、4和21h,用自动伽马计数器计算肿瘤和正常组织种211At的活性。结果以每个器官(%ID)和每克组织的注射剂量百分比表示(%ID/g)。由图2可知,iso-211At-SAGMB-VHH_1028的肿瘤摄取量在1h时为10.28 ± 0.90% ID/g,4h时为10.21±3.10% ID/g,21小时时降至4.00±1.90% ID/g。且观察到放射性从正常器官快速清除,其中肾脏中的211At水平从1h时的34.20 ± 13.63% ID/g下降到4h时的4.46 ± 0.62% ID/g。
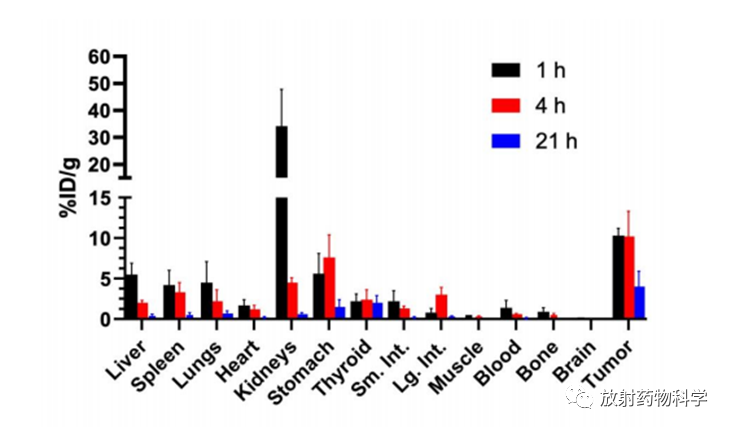
图2. Iso-211At-SAGMB-VHH_1028在皮下BT474异种移植的裸鼠体内的生物分布。
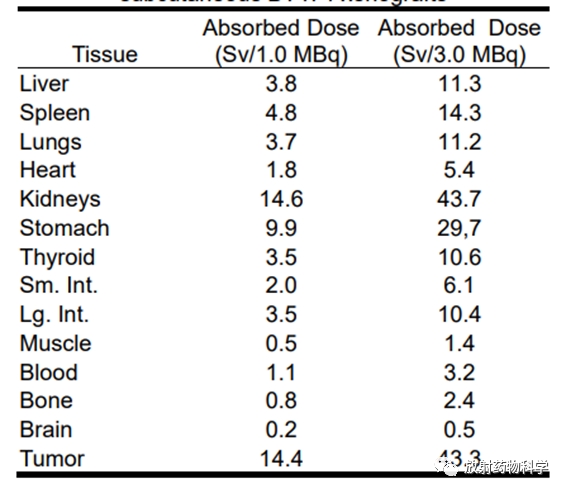
表1列出了从iso-211At-SAGMB-VHH_1028生物分布数据中计算出来的辐射吸收剂量,包括1.0MBq和3.0MBq两种剂量。肿瘤吸收剂量估计为14.4Sv/MBq,高于除肾脏(14.6Sv/MBq)外所有正常组织的计算值。在3.0MBq时,估计肿瘤接受的辐射剂量为43.3Sv。
表1 在皮下注射BT474异种移植的裸鼠中,iso-211At-SAGMB-VHH_1028的估计吸收剂量
抗肿瘤疗效:
iso-211At-SAGMB-VHH_1028疗效研究。单剂量iso-211At-SAGMB-VHH_1028用于BT474异种移植的裸鼠中治疗时,所有治疗组都观察到明显的肿瘤生长延迟(P<0.0001),且存在剂量依赖(图4A)。对于单剂量iso-211At- SAGMB-VHH_1028,接受3.0MBq的11只小鼠中的8只、接受1.9MBq的12只小鼠中的3只,以及接受1.0MBq的10只小鼠的肿瘤完全消退,分别在接受3.0、1.9和1.0MBq剂量的11只、12只和10只动物中看到>50%的肿瘤体积消退(图4B)。所有治疗组都观察到明显的生存获益。单剂iso-211At-SAGMB-VHH_1028使中位生存期从50.5天(对照组)增加到209天(3.0MBq组)(图4C)。在治疗组和对照组之间,体重(图4D)或其他临床上可观察到的毒性迹象没有明显差异。
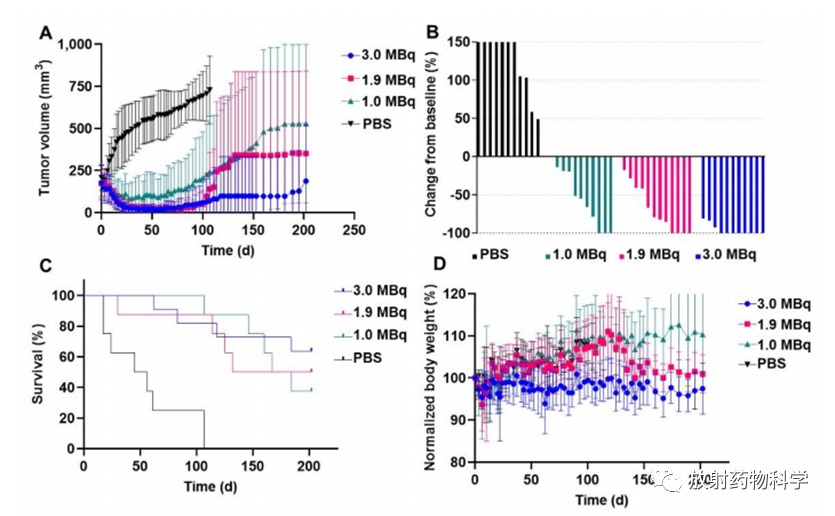
图4. 单剂量iso-211At-SAGMB-VHH_1028对患有BT474异种移植的无胸腺小鼠的疗效。(A)肿瘤体积,(B)最大肿瘤反应瀑布图,(C)Kaplan-Meier曲线,(D)体重监测。
iso-211At-SAGMB-VHH_1028治疗效果的特异性研究。通过与HER2不反应的iso- 211At-SAGMB-VHH_2001对照组直接比较,可评估iso-211At-SAGMB-VHH_1028治疗效果的特异性。单个小鼠肿瘤体积的Spaghetti图(图5A)和最大肿瘤反应的瀑布图(图5B)表明HER2特异性的iso-211At-SAGMB-sdAb结合物可使肿瘤生长明显延迟:在1.0MBq剂量下,11只小鼠中有6只显示肿瘤消退>50%,4只小鼠没有出现肿瘤。相比之下,在接受iso-211At-SAGMB-sdAb对照的动物中没有看到肿瘤生长延迟。如图5C所示,PBS组(44天)和iso-211At-SAGMB-sdAb对照组(34天)的中位生存期没有明显差异。HER2特异性iso-211At-SAGMB-VHH_1028结合物有明显的生存优势,中位生存期为159天,而PBS组为44天。在治疗组和对照组之间,体重(图5D)或其他临床可观察到的毒性迹象没有明显差异。
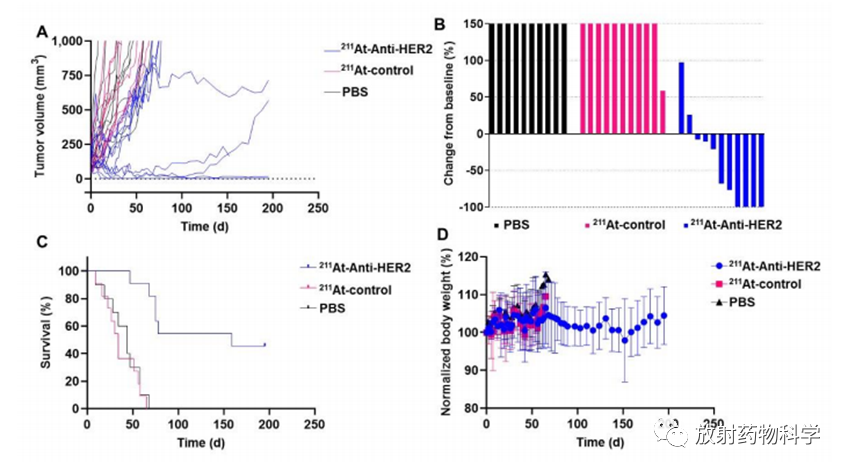
图5. 单剂量iso-211At-SAGMB-VHH_1028和HER2-无关的iso-211At-SAGMB-VHH_2001对患有BT474异种移植的无胸腺小鼠的疗效。(A)单个小鼠的肿瘤体积,(B)最大肿瘤反应瀑布图,(C)Kaplan-Meier曲线,(D)归一化体重。
研究结果:
1. 本研究的结果证实了TAT治疗癌症的潜在优势。在同一BT474异种移植模型中,单剂量的iso-211At-SAGMB-VHH_1028比每周4次的iso-131I-SGMIB-VHH_1028结合物疗效更好。
2. 单剂量iso-211At-SAGMB-VHH_1028即使在研究的最低剂量水平(1.0MBq),中位生存期也增加了361%,从44天到159天,11只动物中有4只肿瘤完全消退,而与HER2-无关的211At-sdAb对照,没有观察到明显的生存期延长。这些反应是在211At活性仅能向肾脏提供14.6Sv时获得的,这一剂量远低于常规外照射的23Gy基准阈值(1Gy=1Sv)。
研究要点:
1. sdAbs由于快速和均匀的肿瘤渗透性,成为TAT的一个有吸引力的载体。
2. 砹-211非常适合用于标记sdAbs。具有以下优势:1)7.2小时的半衰期与标记的sdAbs在人体中约8小时的生物清除半衰期很匹配。2)与213Bi和225Ac相比,211At的肾脏摄取更少,肾脏毒性的风险较低。3)211At每次衰变只发射一个粒子,没有发射子体;4)211At能以合理的成本提高可用性。
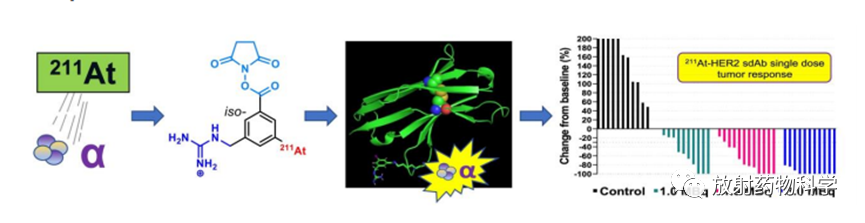
全文结论:
单剂量的iso-211At-SAGMB-抗HER2-sdAb的TAT,能够有效抑制HER2高表达乳腺癌小鼠的肿瘤、延迟荷瘤鼠生存期,未见明显正常组织毒性。
这种TAT策略值得进一步研究用于治疗HER2高表达的癌症患者,为传统HER2靶向疗法没有疗效响应的患者提供一个潜在的新型治疗方案。
靳桐 译
Dr. Yutian Feng、卓巍彬 校对
译者单位简介:砹尔法纽克莱(宁波)医疗科技公司成立于2020年11月,落地于浙江省宁波市杭州湾新区。专注于医用核素及核素药的生产研发,为疾病提供诊断及治疗为一体(Radiotheranostic)的治疗方案。利用全球领先的阿尔法核素211At–砹技术,实现癌症精准医疗。
Citation:Feng Y, Meshaw R, Zhao XG, Jannetti SA 3rd, Vaidyanathan G,Zalutsky MR. Effective Treatment of Human Breast Carcinoma Xenografts withSingle-Dose 211At-Labeled Anti-HER2 Single Domain Antibody Fragment. J NuclMed. 2022 May 26:jnumed.122.264071. doi: 10.2967/jnumed.122.264071. Epub aheadof print. PMID: 35618478.
相关文章: